【アニメーション・練習問題付き】イオン結晶・金属結晶・分子結晶・共有結合の結晶(共有結晶)の違いを説明できますか?本記事では、それぞれの結晶でよく出題される特徴の解説と、どの結晶に分類されるかを選択する問題の解き方を具体例(入試問題)とともに詳しく解説します。
ちなみに僕は10年以上にわたりプロとして個別指導で物理化学を教えてきました。
おかげさまで、個別指導で教えてきた生徒は1000名以上、東大京大国公立医学部合格実績は100名以上でして、目の前の生徒だけでなく、高校化学で困っている方の役に立てればと思い、これまでの経験をもとに化学の講義をまとめています。参考になれば幸いです。
イオン結晶とは

イオン結合による結晶です。多数の陽イオンと陰イオンが規則正しく配列して固体に
なっています。化学式は組成式で表します。
詳しくは イオン結合とは?組成式や共有結合との違いなど具体例で解説 を参照してください。
イオン結晶の見分け方
金属元素と非金属元素が含まれた物質はイオン結晶です。例えば、NaCl,MgSO4など。
例外として、アンモニウムイオンNH4+を含む場合もイオン結晶です。例えば、NH4Cl,(NH4)2SO4など。
融点・沸点
クーロン力(静電気力)がかなり強いので,融点・沸点はかなり高いです。
機械的性質
クーロン力(静電気力)がかなり強いので硬いです。
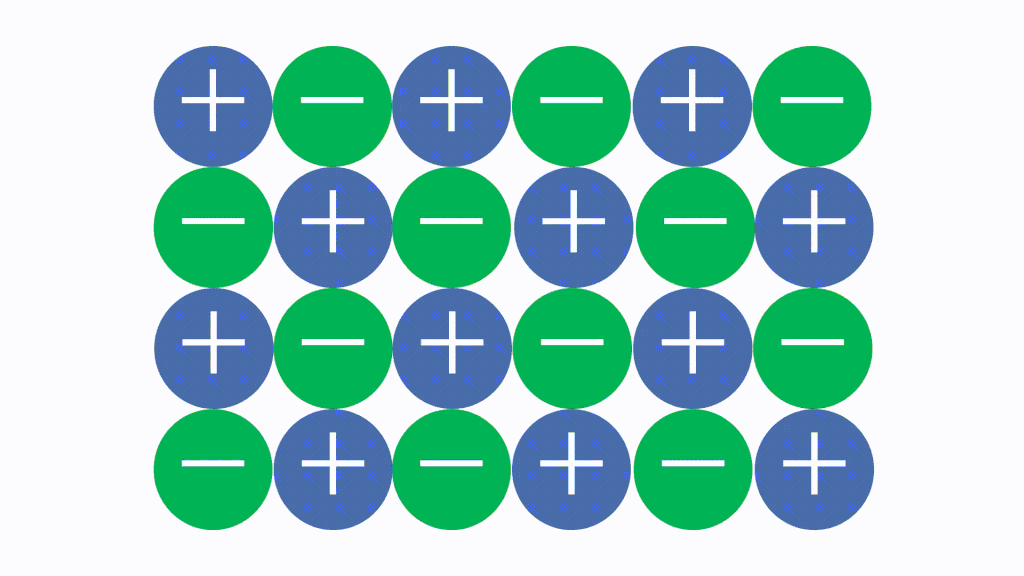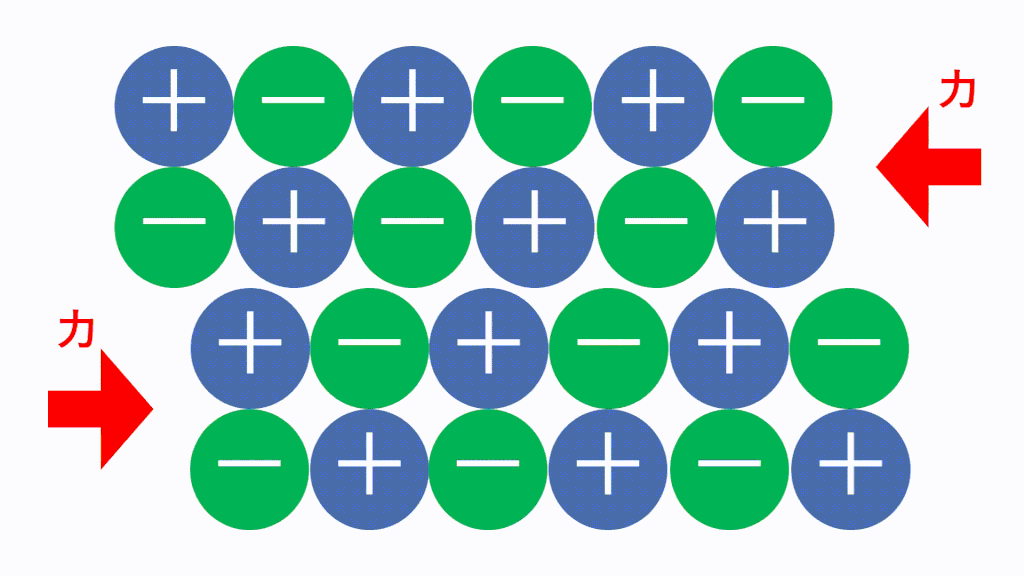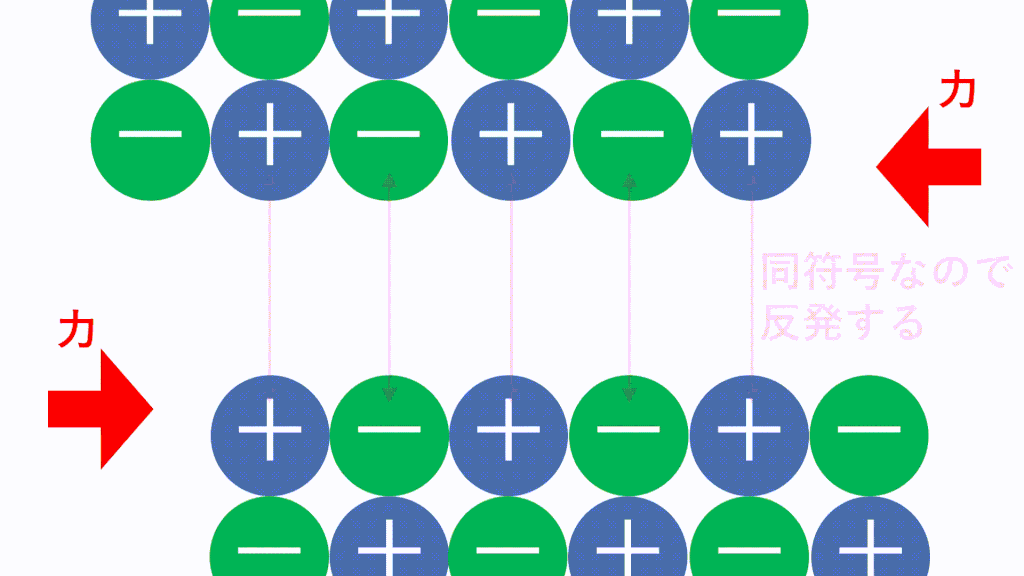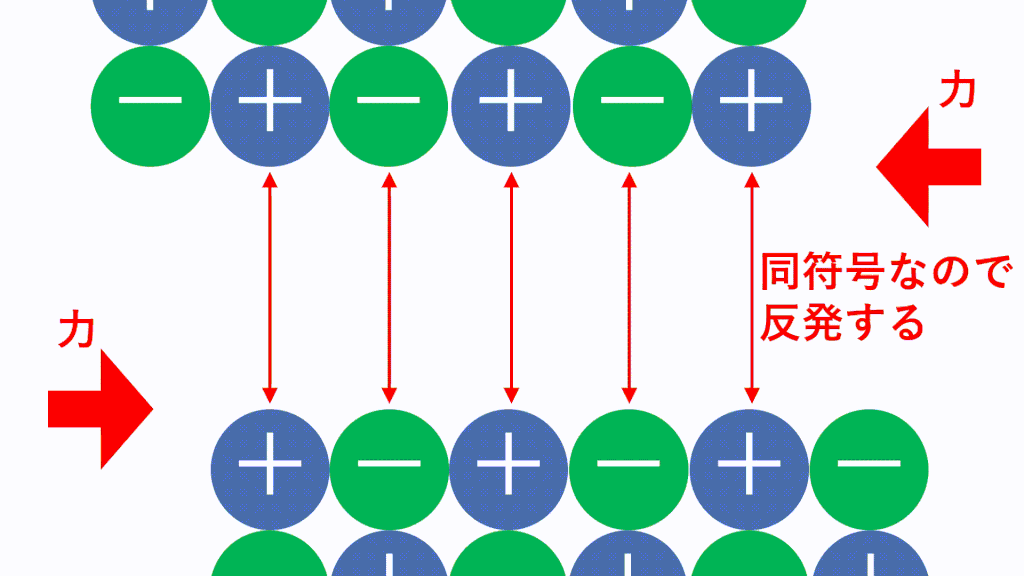
ただし、強い外力により簡単に割れます(配列がずれると反発力が働くから)。
電気伝導性
固体ではイオンの位置が固定されており電導性はありませんが、融解液や水溶液ではイオンが動けるようになり,電気伝導性があります。(液体状態は流動性があるから)
・「融ける」は固体から液体に状態変化(融解)することです。氷が“融ける”という使い方です。
・「溶ける」は固体が液体に溶ける(溶解)ことです。食塩が水に“溶ける”という使い方です。
金属結晶とは

金属結合による結晶です。多数の金属が自由電子により結びついています。
化学式は組成式で表します。
イオン結晶の見分け方
金属元素のみが含まれた物質は金属結晶です。例えば、Ag,Na,Au,Feなど金属の単体です。
融点・沸点
典型元素-多様(アルカリ金属,Hgなどは低い)
遷移元素-かなり高い
機械的性質
展性(二次元的) Au>Ag>Pt>…,
延性(一次元的) Au>Ag>Cu>…
(例外Hgは液体)
電気伝導性
よく導きます。しかし、高温になるほど金属原子の熱運動が激しくなり,自由電子が結晶中を通過しにくくなり電気抵抗が大きくなります。
共有結合の結晶(共有結晶)とは

共有結合が際限なく続くことによってできた結晶です。
化学式は組成式で表します。
黒鉛が例外だらけになっている理由に関しては、 黒鉛(グラファイト)とダイヤモンドの違いと性質 を参照してください。
共有結合の結晶(共有結晶)の見分け方
大学受験で覚えておくべき物質はC,Si,SiO2,SiCの4種類のみです。
融点・沸点
共有結合が非常に強いので,非常に高いです。
機械的性質
共有結合が非常に強いので,極めて硬いです。
ただし、黒鉛のみ薄くはがれやすく,軟らかいです。
電気伝導性
電気伝導性はありません。
ただし、黒鉛のみ電気伝導性があります。
分子結晶とは

非金属のみで構成されます。
いくつかの非金属原子が共有結合により結合して分子になり,その分子がさらに分子間力によって多数結合して固体になったものです。
化学式は分子式で表します。
分子結晶の見分け方
共有結晶となるC,Si,SiO2,SiC以外の非金属元素のみから構成されているものが分子結晶です。例えば、ドライアイスCO2 ,ナフタレンC10H8,ヨウ素I2などです。
融点・沸点
分子間力が弱いので融点・沸点は低いです。昇華しやすいものが多いです。
機械的性質
分子間力が弱いので軟らかいです。
電気伝導性
電気伝導性はありません。
結晶の見分け方まとめ
金属単体 ・・・ 金属結晶 (具体例:Au、Fe、Ptなどの金属単体)
金属と非金属が両方含まれた物質 ・・・ イオン結晶(NaCl、MgCl2、BaSO4など金属元素と非金属元素両方が含まれている)
NH4+を含む非金属物質 ・・・ イオン結晶(NH4Clなど)
C、Si、SiO2、SiCのどれか ・・・ 共有結晶
それ以外非金属のみ ・・・ 分子結晶(上を先に選んでから消去法で考えるとよいです)
と見分けましょう。
結晶の分類の入試問題例
例題(金沢大)
結晶は粒子間の結合の仕方で4種類に大別される。
(1) イオン結晶 (2) 共有結合の結晶 (3) 分子結晶 (4) 金属結合結晶
下のA群にはそれぞれの結晶を構成する粒子の種類が,B群にはその粒子間を結びつけている結合力の種類が,C群には4種類の結晶の特徴的な性質が,D群には各種の結晶の実例が示してある。各群の中から,上の(1)~(4)に対応するものを選んで記号で答えよ。ただしD群からは2個ずつ選べ。
A群
(ア) 原子 (イ) 分子 (ウ) 原子と自由電子 (エ) 陽イオンと陰イオン
B群
(オ) 自由電子による結合 (カ) 静電気的な引力
(キ) 電子対の共有による結合 (ク) ファンデルワールス力
C群
(ケ) 極めて硬く,融点も高い。 (コ) 展性・延性を有し,電気伝導性がよい。
(サ) 電気伝導性はないが,水溶液や融解状態では電気を伝導する。
(シ) 一般に軟らかく,融点が低い。昇華性を示すものもある。
D群
(a) ヨウ素 (b) 塩化鉄(Ⅲ) (c) ナトリウム (d) 臭化カリウム
(e) クロム (f) 炭化ケイ素 (g) ドライアイス (h) ダイヤモンド
【解答】
(1) エ,カ,サ,b,d (2) ア,キ,ケ,f,h
(3) イ,ク,シ,a,g (4) ウ,オ,コ,c ,e
【解説】
A群:(1)イオン結晶が(エ)陽イオンと陰イオンから構成されていることはすぐわかります。自由電子というキーワードから(4)金属結晶が(ウ)原子と自由電子から構成されていることがわかります。(3)分子結晶は(イ)分子から構成されています。そのため、残りの(2)共有結合の結晶は(ア)原子からなることが選べます。
B群:先ほどと同様に、自由電子というキーワードから(オ)自由電子による結合は(4)金属結晶です。共有というキーワードから(キ)電子対の共有による結合は(2)共有結合の結晶です。(ク)ファンデルワールス力は分子間力の一種なので(3)分子結晶です。そのため、残りの(カ)静電気的な引力は、陽イオンと陰イオンの間の静電気力のことなので(1)イオン結晶が選べます。
C群:展性・延性というキーワードから(コ)が(4)金属結晶です。電気伝導性はないが,水溶液や融解状態では電気を伝導するのはイオン結晶の特徴なので(サ)が(1)です。ちなみに、強い外力で簡単に割れるということも頻出です。昇華性というキーワードから(シ)が(3)です。そのため、残りの(ケ)はやっぱり(2)の共有結晶です。
D群:
(4)金属結晶は金属のみから構成される金属単体なので、(c) ナトリウムと(e) クロムです。イオン結晶は金属元素と非金属元素から構成される物質なので、(b) 塩化鉄(Ⅲ)と(d) 臭化カリウムです。共有結合の結晶は、C,Si,SiO2,SiCなので(f) 炭化ケイ素と(h) ダイヤモンドです。分子結晶はC,Si,SiO2,SiC以外の非金属元素のみからなる物質なので、(a) ヨウ素と(g) ドライアイス です。
[/su_spoiler]さいごに
本記事でご紹介した例題は非常に重要な問題です。
結晶4種類の性質を覚え、具体例の選び方をわかっていないと答えられない問題となっており、この単元の理解を確かめるのに有効な問題ですので、お気に入りに登録するなどして、覚えるまで何度も復習しましょう。ちなみに復習はタイミングが命です。僕がこれまで1000名以上の個別指導で、生徒の成績に向き合ってきた経験をもとにまとめた化学の勉強法に記載しているので、こちらも参考にしてもらえれば幸いです。
また、本記事をググってくださったときのように、参考書や問題集を解いていて質問が出たときに、いつでもスマホで質問対応してくれる塾はこれまでありませんでした。
しかし、2020年より駿台がこの課題を解決してくれるサービスmanaboを開始しました。今のところ塾業界ではいつでも質問対応できるのは駿台だけかと思います。塾や予備校を検討している方の参考になれば幸いです。