イオン結合は陽イオンと陰イオンとの間に働く静電気力(クーロン力)により生じます。入試で出題頻度も高いイオン結合と共有結合の違いとは何で、どのように見分けるのか、組成式と分子式の違いについて具体的かつ丁寧に解説します。
ちなみに僕は10年以上にわたりプロとして個別指導で物理化学を教えてきました。
おかげさまで、個別指導で教えてきた生徒は1000名以上、東大京大国公立医学部合格実績は100名以上でして、目の前の生徒だけでなく、高校化学で困っている方の役に立てればと思い、これまでの経験をもとに化学の講義をまとめています。参考になれば幸いです。
イオン結合とは
陽イオンと陰イオンとの間に働く静電気力による結合をイオン結合といいます。
金属原子と非金属原子が結合するときに生じます。
ただし例外として、アンモニウムイオンNH4+を含むときは非金属原子のみで構成されていてもイオン結合です。
結合の仕組み
陽イオンと陰イオンはプラスとマイナスなので、お互いに引き合います。この静電気的な引力をクーロン力といい、このクーロン力で結びついた結合がイオン結合です。
単原子イオン … 金属元素(Na+,Ca2+など)
多原子イオン … NH4+のみ
単原子イオン … 非金属元素(Clー,O2ーなど)
多原子イオン … NH4+以外(SO42ー,OHーなど)
例えば、NaClやMgO,K2SO4など金属元素と非金属元素が組み合わさってできたものがイオン結合性の物質ということです。
繰り返しますが、イオン結合とは、陽イオンと陰イオンの間のクーロン力(静電気力)で結びつきます。そのため、以下の図のようにいくつもの陽イオンと陰イオンが互いに際限なく結合を繰り返すことで結晶となり、物質を構成していきます。
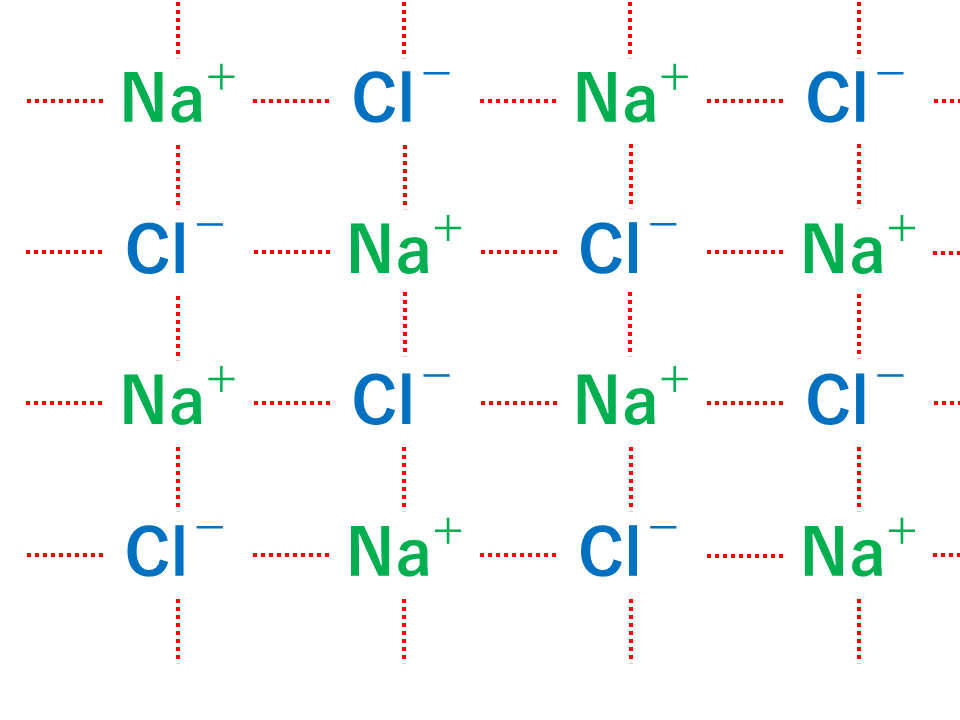
イオン結合と共有結合の違い
上の図からわかるとおり、
イオン結合は、プラスとマイナスの間で生じるクーロン力によって作られており、陽イオンと陰イオンがある限り際限なく結合し続けます。
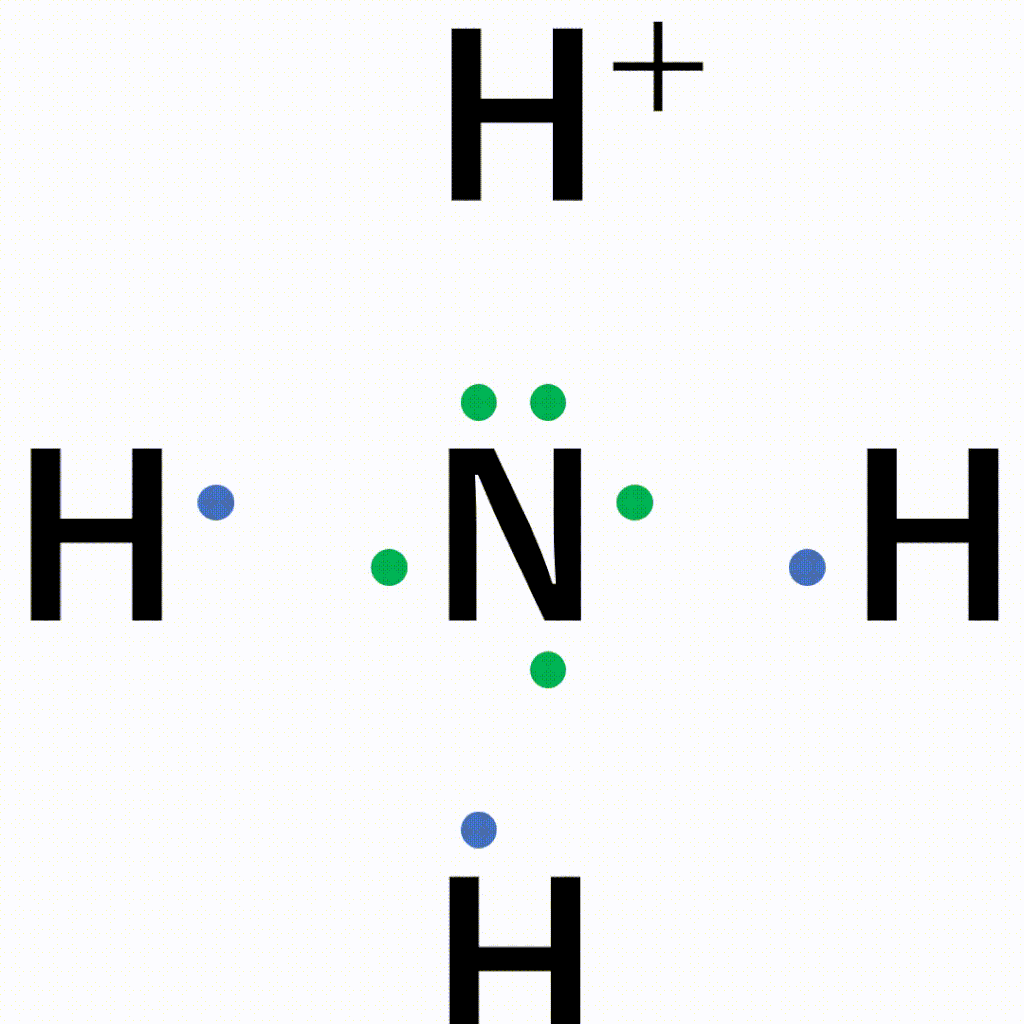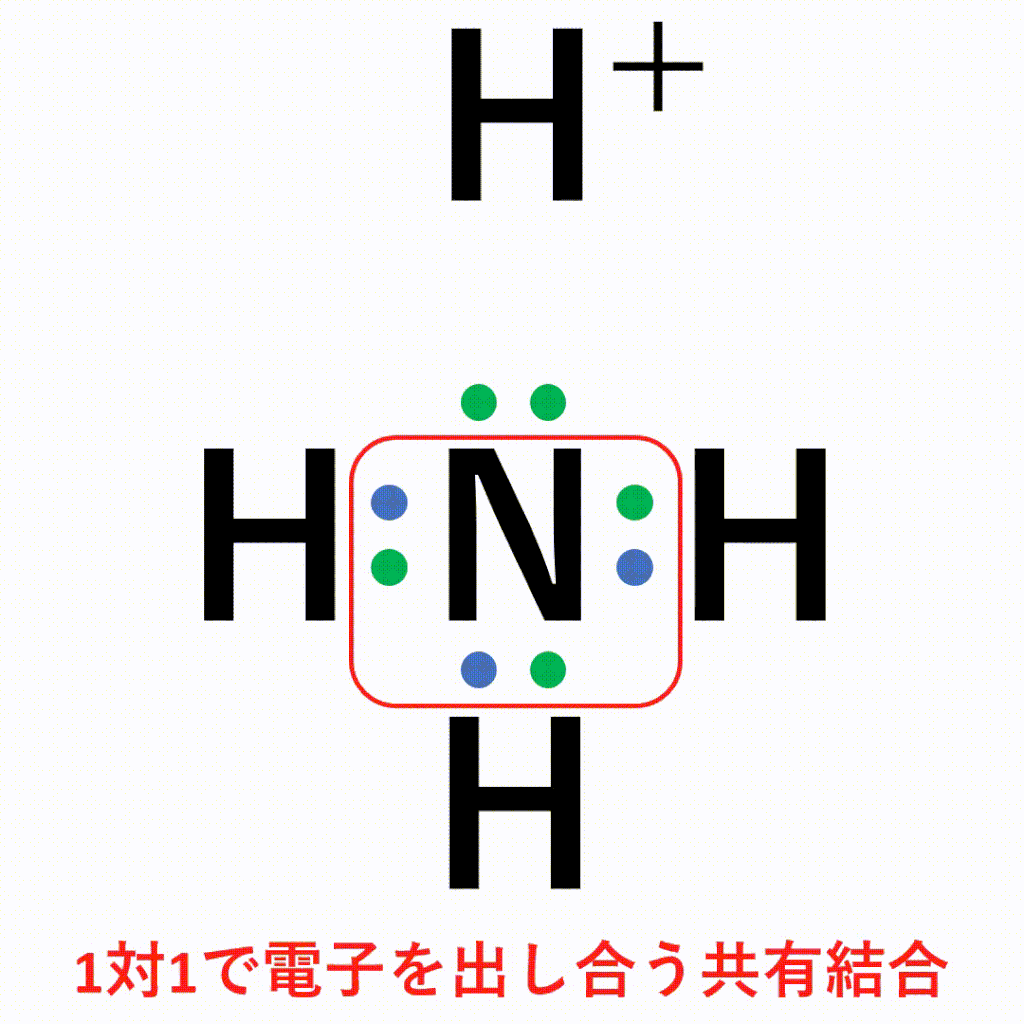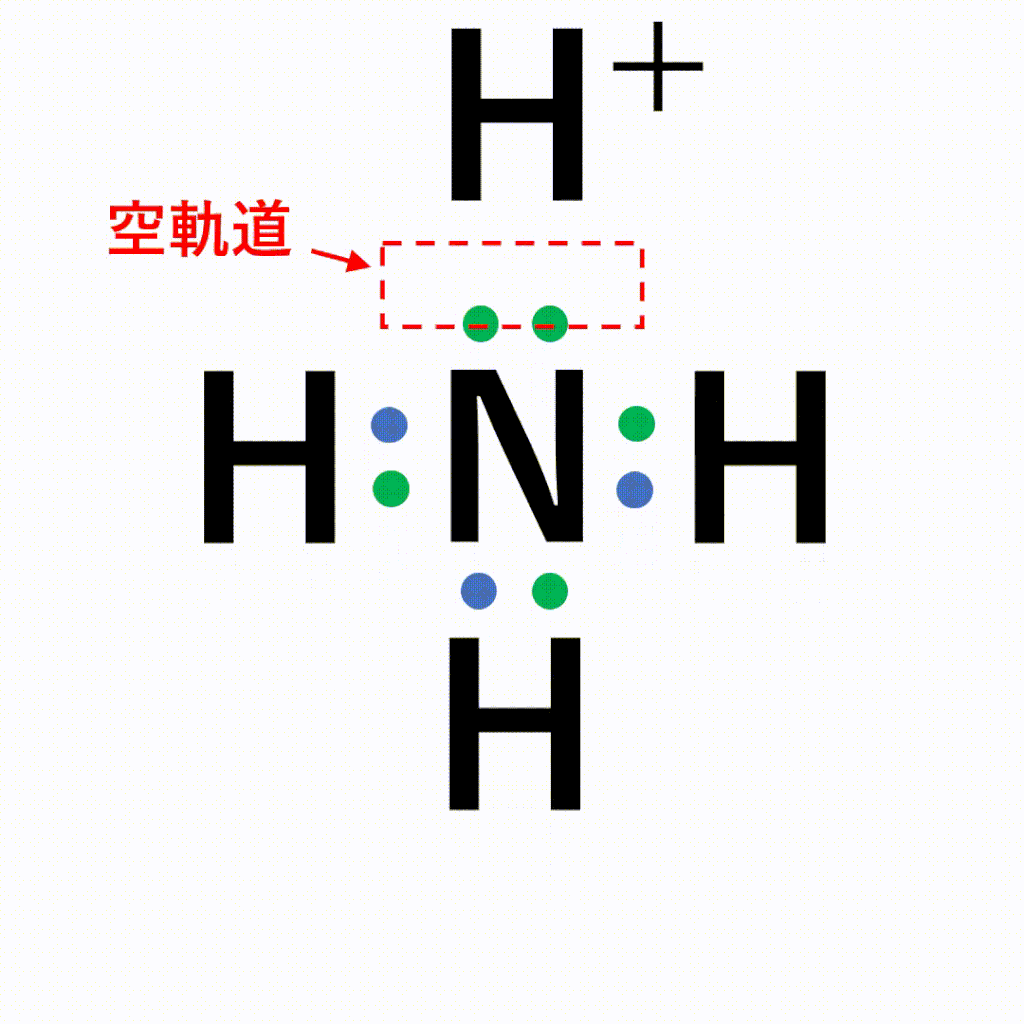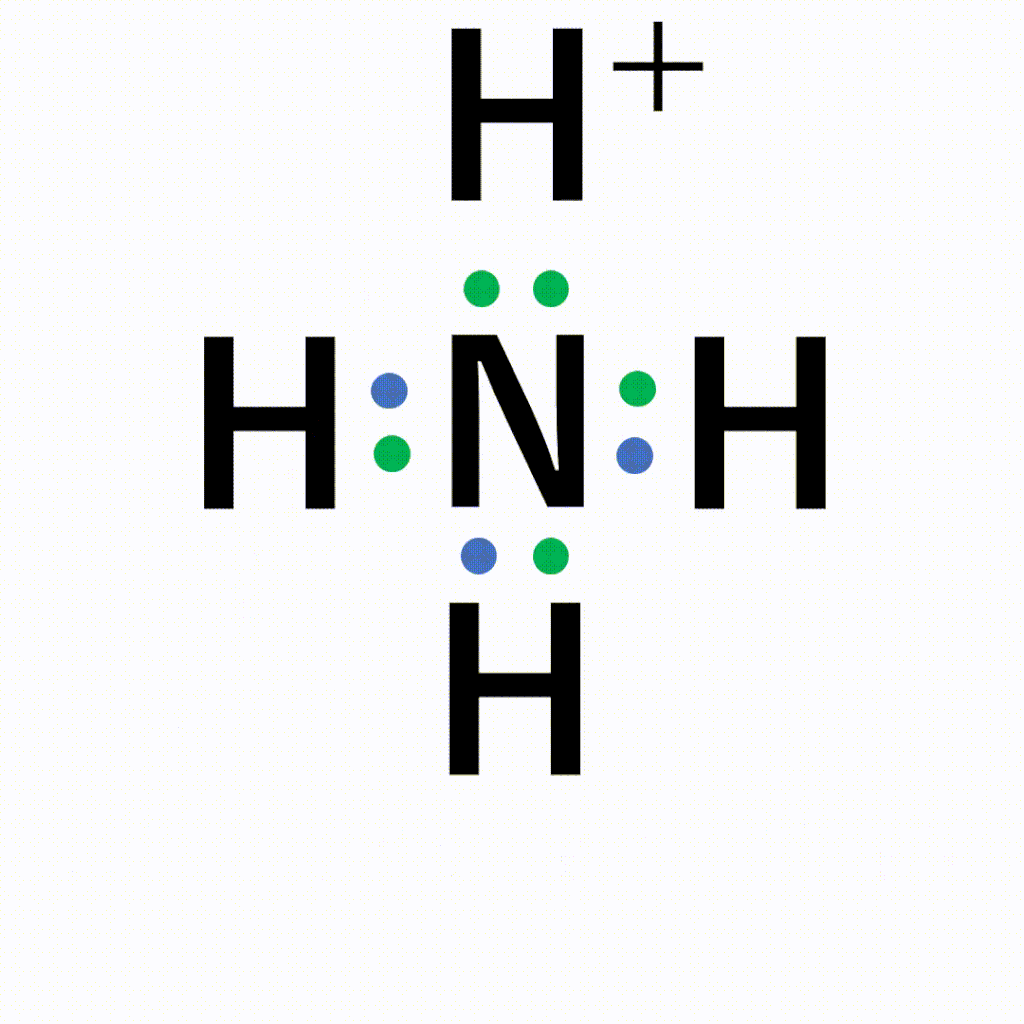
それに対し、共有結合はお互いが持つ電子を出し合うことで結合を作っており、電子の数には制限があるため、ひとつのかたまり(=分子)が形成されます。
ただし、共有結合の結晶は例外です。
組成式と分子式の違い
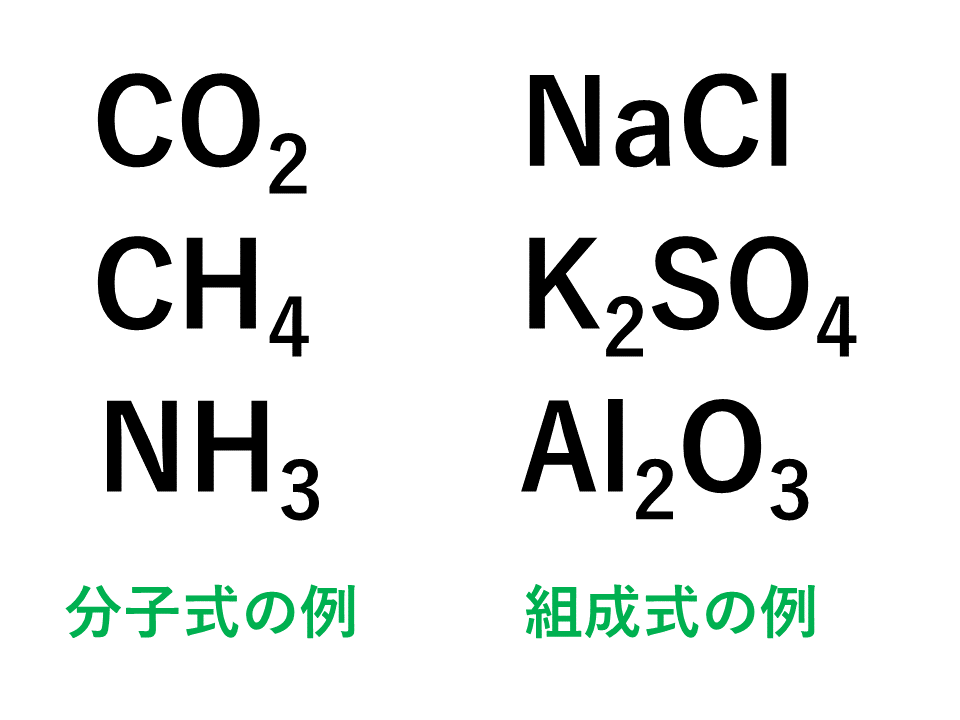
共有結合によって作られた分子を表す分子式は、ひとつのかたまり(=分子)に使われている原子の個数を表したものでした。
例えば、CO2であればC原子1個とO原子2個が結合してひとつのかたまりとなった分子ということでした。
参考
【アニメーション解説】共有結合とは?二酸化炭素などの例を図で完全解説
これに対し、イオン結合によって作られた物質は、陽イオンと陰イオンが際限なく結合して構成されているため、分子のようにひとつのかたまりの状態になっていません。そのため、陽イオンと陰イオンの数を最も簡単な整数比にした組成式というものを使って表します。
例えば、
塩化ナトリウムであれば、Na+:Cl- = 1:1の割合で結合しているため、NaClと書きます。
硫酸カリウムであれば、K+:SO42- = 2:1 の割合で結合しているため、K2SO4と書きます。
酸化アルミニウムであれば、Al3+:O2- = 2:3 の割合で結合しているため、Al2O3と書きます。
それでは組成式の作り方を説明します。
⇒ 受験で覚えておくべき単原子イオン・多原子イオンの一覧 で覚えましょう!!(2)陽イオンの価数と陰イオンの価数を足し合わせてゼロになるように組み合わせます。
塩化ナトリウム
Na+の価数が+1,Cl- の価数が-1なので1:1で結合し、NaClとなります。
硫酸カリウム
K+の価数が+1,SO42- の価数が-2なので、K+が2個、SO42-が1個だとプラスマイナスゼロとなります。
よって、K2SO4と書きます。
酸化アルミニウム
Al3+の価数が+3,O2- の価数が-2なので、Al3+が2個、O2-が3個だとプラスマイナスゼロとなります。
よって、Al2O3と書きます。
硫酸アルミニウム
Al3+の価数が+3,SO42- の価数が-2なので、Al3+が2個、SO42-が3個だとプラスマイナスゼロとなります。
よって、Al2(SO4)3 と書きます。
※Al2SO43 と書かないように注意しましょう。これだとO原子が43個という意味になってしまいます。あくまでもS原子1個とO原子4個から構成されるSO42-が3セット必要という意味なので括弧が必要です。
さいごに
イオン結合を理解するには、結局イオンの価数をしっかりと覚えておかないと話にならないことが分かったと思います。まだ覚えられていないひとは、 受験で覚えておくべき単原子イオン・多原子イオンの一覧に記載しているイオンは必ず覚えておきましょう。
なお、暗記の復習はタイミングが極めて重要なので、復習のタイミングについて詳しく知りたい方は、僕がこれまで1000名以上の個別指導で、生徒の成績に向き合ってきた経験をもとにまとめた化学の勉強法も参考にしてもらえれば幸いです。
また、本記事をググってくださったときのように、参考書や問題集を解いていて質問が出たときに、いつでもスマホで質問対応してくれる塾はこれまでありませんでした。
しかし、2020年より駿台がこの課題を解決してくれるサービスmanaboを開始しました。今のところ塾業界ではいつでも質問対応できるのは駿台だけかと思います。塾や予備校を検討している方の参考になれば幸いです。